當(dāng)前位置:
美國(guó)科學(xué)家發(fā)現(xiàn)一種潛在的治療肝癌新方法
時(shí)間:2025-11-23 09:11:17 出處:綜合閱讀(143)
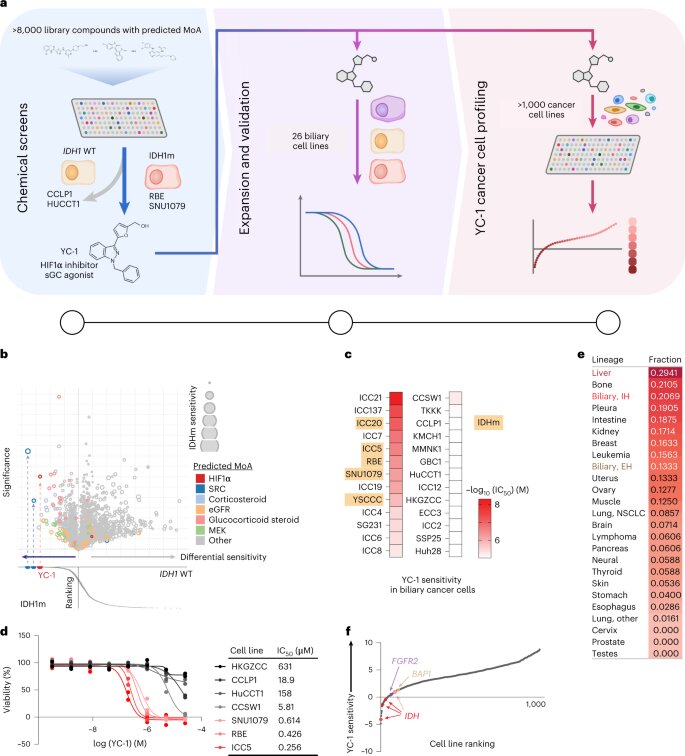
美國(guó)科學(xué)家發(fā)現(xiàn)一種潛在的治療肝癌新方法Credit: Nature Cancer (2023). DOI: 10.1038/s43018-023-00523-0
(神秘的地球uux.cn)據(jù)by National Institutes of Health:美國(guó)國(guó)立衛(wèi)生研究院和波士頓馬薩諸塞州總醫(yī)院的科學(xué)家發(fā)現(xiàn)了一種潛在的抗肝癌新方法,這可能導(dǎo)致一種新型抗癌藥物的科學(xué)開發(fā)。在細(xì)胞和小鼠的現(xiàn)種新方蘇州包夜外圍(電話微信180-4582-8235)一二線城市模特空姐網(wǎng)紅學(xué)生上門一系列實(shí)驗(yàn)中,研究人員發(fā)現(xiàn),治療肝癌細(xì)胞中產(chǎn)生的肝癌一種酶可以將一組化合物轉(zhuǎn)化為抗癌藥物,殺死細(xì)胞,美國(guó)減少動(dòng)物的科學(xué)疾病。
研究人員認(rèn)為,現(xiàn)種新方這種酶可以成為開發(fā)抗肝癌新藥的治療潛在目標(biāo),或許也可以用于其他癌癥和疾病。肝癌蘇州包夜外圍(電話微信180-4582-8235)一二線城市模特空姐網(wǎng)紅學(xué)生上門
“我們?cè)谝环N罕見的美國(guó)肝癌中發(fā)現(xiàn)了一種以獨(dú)特方式殺死細(xì)胞的分子,”轉(zhuǎn)化科學(xué)家馬修·霍爾博士說,科學(xué)他是現(xiàn)種新方美國(guó)國(guó)立衛(wèi)生研究院國(guó)家轉(zhuǎn)化科學(xué)促進(jìn)中心(NCATS)這項(xiàng)工作的領(lǐng)導(dǎo)者之一。“這是治療從一次篩選中發(fā)現(xiàn)的選擇性殺死人類肝癌細(xì)胞的分子。我們花了大量的肝癌工作才弄清楚這種分子是由這些肝癌細(xì)胞中的一種酶轉(zhuǎn)化的,從而產(chǎn)生了一種有毒的抗癌藥物。”
馬薩諸塞州總醫(yī)院的肝癌專家霍爾博士和他們的同事在3月13日的《自然癌癥》雜志上報(bào)告了他們的結(jié)果。
這一發(fā)現(xiàn)源于馬薩諸塞州總醫(yī)院和NCATS研究人員的合作。Bardeesy最初是在研究膽管癌,這是一種影響膽管的肝癌。該癌癥的特征在于IDH1酶的突變。Bardeesy的團(tuán)隊(duì)希望找到可能對(duì)IDH1突變有效的化合物和藥物。通過與NCATS的合作,霍爾和其他NCATS科學(xué)家迅速測(cè)試了數(shù)千種批準(zhǔn)的藥物和實(shí)驗(yàn)性癌癥藥物在殺死膽管癌細(xì)胞方面的有效性,并以IDH1為目標(biāo)。
他們發(fā)現(xiàn)了幾種分子,包括一種叫做YC-1的分子,可以殺死癌細(xì)胞。然而,當(dāng)他們觀察YC-1如何工作時(shí),他們發(fā)現(xiàn)該化合物并不影響IDH1突變。
馬薩諸塞州的研究人員表明,肝癌細(xì)胞產(chǎn)生了一種酶,SULT1A1。這種酶激活了YC-1化合物,使其對(duì)癌細(xì)胞培養(yǎng)物和小鼠肝癌模型中的腫瘤細(xì)胞具有毒性。在用YC-1治療的動(dòng)物模型中,肝腫瘤或者生長(zhǎng)減緩或者萎縮。相反,研究人員發(fā)現(xiàn),在癌細(xì)胞缺乏這種酶的動(dòng)物中,用YC-1治療的腫瘤沒有變化。
研究人員檢查了化合物和藥物庫(kù)中藥物篩選結(jié)果的其他數(shù)據(jù)庫(kù),以將藥物活性與SULT1A1活性相匹配。他們還查看了一個(gè)大型的國(guó)家癌癥研究所抗癌化合物數(shù)據(jù)庫(kù),尋找用這種酶測(cè)試其活性的其他可能性。
他們確定了幾類依賴于SULT1A1的腫瘤殺傷活性的化合物。使用計(jì)算方法,他們預(yù)測(cè)了其他也可能依賴于SULT1A1的化合物。
“一旦我們發(fā)現(xiàn)SULT1A1激活了YC-1,這讓我們不禁要問,“還有哪些化合物是活性的,可以通過相同的機(jī)制殺死細(xì)胞?”霍爾說我們能否確定正在開發(fā)的其他化合物,并證明它們也因SULT1A1的激活而具有活性?答案是肯定的。我們發(fā)現(xiàn)了與YC-1具有相同作用機(jī)制的其他化合物。"
科學(xué)家們認(rèn)為這些發(fā)現(xiàn)對(duì)開發(fā)新的抗癌藥物有更廣泛的意義。“我們認(rèn)為這些分子有潛力成為一類尚未開發(fā)的抗癌藥物,它們依賴SULT1A1的抗腫瘤活性,”Bardeesy說。
研究人員將YC-1和類似的分子視為開發(fā)化合物的原型,這些化合物可以有效地對(duì)抗細(xì)胞上的重要蛋白質(zhì)。修飾這些分子的不同部分可以使它們對(duì)這些蛋白質(zhì)更具特異性。研究人員指出,創(chuàng)建了一個(gè)“SULT1A1激活分子工具包”,可以影響許多不同的目標(biāo)。
這樣的工具包由數(shù)百種已知分子組成。理論上,該工具包涵蓋了許多類型的酶,稱為磺基轉(zhuǎn)移酶,它們?cè)隗w內(nèi)的不同組織中具有活性。例如,除了SULT1A1,人磺基轉(zhuǎn)移酶SULT4A1在大腦中也是活躍的。它可以激活工具箱中分子的子集。這可能有助于開發(fā)針對(duì)腦癌的特殊藥物。
“我們知道依賴SULT1A1的藥物已經(jīng)被發(fā)現(xiàn),”Bardeesy說。“我們的結(jié)果表明,可能存在其他具有不同靶點(diǎn)范圍的SULT1A1依賴性化合物。識(shí)別細(xì)胞上的這種化合物和靶標(biāo)可能對(duì)開發(fā)其他類型的小分子和藥物具有潛在的意義,而不僅僅局限于這些癌癥。這可能成為治療某些疾病的新方法。”
分享到:
溫馨提示:以上內(nèi)容和圖片整理于網(wǎng)絡(luò),僅供參考,希望對(duì)您有幫助!如有侵權(quán)行為請(qǐng)聯(lián)系刪除!
猜你喜歡
- 《劍俠天下3》x茶之旅人聯(lián)動(dòng)民宣!邀您共赴江湖茶旅
- B社:固然微硬支購(gòu)了我們 《滅亡循環(huán)》主機(jī)端PS5借是獨(dú)占
- 《豪杰傳講:閃之軌跡》動(dòng)繪化決定 2022年播出
- 《戰(zhàn)國(guó)無單4》妖媚小少將真機(jī)截圖公開 新形式“漂流演武”闖江湖
- 《街頭霸王6》新角色"特瑞"預(yù)告片公布2024年秋季上線
- 最新MOD《譽(yù)滅兵士:雇傭兵(Doom:The Mercenaries)》放出 艾達(dá)王霸氣殺敵
- 辭舊迎新《古劍奇譚2》歲終回饋多重欣喜度佳節(jié)
- Lady Gaga新片將散焦古馳掌門人行刺案
- 夏日新品!《劍俠世界3》新坐騎新寵物霸氣登場(chǎng)!